Cuba presentará a OMS resultados de sus vacunas anti COVID-19
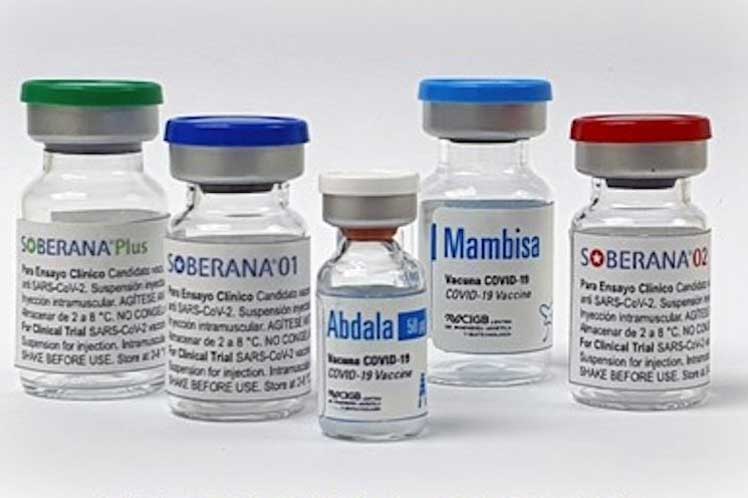
Cuba anunció que mostrará a la Organización Mundial de la Salud (OMS) los resultados de sus vacunas anti COVID-19 Soberana 02 y Abdala, esta última autorizada para uso de emergencia.
En conferencia de prensa este viernes, el doctor Eduardo Martínez, presidente del grupo BioCubaFarma, aseguró que continuará la comunicación permanente con las representaciones de la OMS y la Organización Panamericana de la Salud en la nación, con vistas a presentar las evidencias científicas recopiladas durante las fases de los estudios clínicos, y al mismo tiempo, publicando en revistas especializadas a nivel internacional.
“Proseguiremos el proceso para alcanzar el registro sanitario de las vacunas y en ese trayecto mantendremos el intercambio con estas organizaciones internacionales”, expresó Martínez.

Asimismo, puntualizó que “el uso de los inmunógenos cubanos en otros países solo dependerá que el receptor emita un permiso de uso de emergencia”.
Por último, precisó que en los próximos días enviarán al Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos (Cecmed), autoridad reguladora cubana, el expediente para la autorización del uso de emergencia del esquema de dos dosis de Soberana 02 más una de Soberana Plus.
La propia entidad, de referencia regional y precalificada por la OMS para el tema de las vacunas, autorizó el uso de emergencia de Abdala, luego de demostrar su alto por ciento de eficiencia.

Sobre Abdala: la vacuna anti Covi2-19
Abdala, la vacuna cubana anti-COVID-19 primera en América Latina y el Caribe con autorizo de uso de emergencia, nació del talento y del esfuerzo de los científicos y trabajadores del Centro de Ingeniería Genética y Biotecnología (CIGB), y hoy es la primera vacuna con autorizo de uso de emergencia, otorgado por el Cecmed.
Esta vacuna, primera de su tipo fabricada por un laboratorio de un país de América Latina y el Caribe, fue descrita como “un hito”, por la directora general de dicha institución científica, doctora Marta Ayala Ávila, al destacar que “el logro se obtuvo a tan solo siete meses del inicio de la evaluación clínica del inmunógeno”.
Sobre el proceso que debe seguirse para lograr la aprobación del Cecmed, Ayala Ávila ofreció detalles que abarcan desde la presentación inicial del expediente maestro de las organizaciones que forman parte del sistema productivo a saber, CIGB, donde se fabrica el ingrediente activo; y Laboratorios AICA, donde se realiza el llenado y envase de la vacuna, paso previo a la inspección que realiza el Cecmed.
Luego de esos dos procesos, y demostrada una eficacia de 92,28 % en la Fase III de ensayos clínicos, se procedió a presentar el expediente para el autorizo de uso de emergencia del fármaco, concedido en horas de la mañana del viernes 9 de julio, por la referida entidad reguladora.
“Con el autorizo de uso de emergencia, estamos en condiciones de extender la vacunación al resto del país y a otras naciones que se han acercado con interés de colaborar y firmar contratos para el suministro del fármaco”, concluyó la científica.
Sobre esquema de vacunación Soberana 02 + Soberana Plus
La evaluación interina del esquema heterólogo de dos dosis del candidato vacunal Soberana 02 más una dosis de Soberana Plus arrojó una eficacia de 91,2 %, según dieron a conocer el pasado jueves, autoridades del Instituto Finlay de Vacunas (IFV).
Al respecto, la investigadora principal del ensayo clínico Fase III de Soberana 02, doctora María Eugenia Toledo Romaní, señaló que, en términos de implementación, el ensayo cumplió con elevados estándares de confiabilidad de datos, monitoreo sistemático de la información y seguimiento de los sujetos, así como en los principios éticos del estudio, garantizados por un Comité de Ética Independiente.
Estos resultados permiten presentar, próximamente, el expediente del esquema Soberana 02 + Soberana Plus al Cecmed, para solicitar el autorizo de uso de emergencia, según explicó el doctor Eduardo Martínez Díaz, presidente de BioCubaFarma, quien añadió que se seguirá trabajando para lograr el Registro Sanitario definitivo de la vacuna Abdala y del candidato Soberana 02, una vez que reciba el autorizo.
“Pensamos que antes de que se acabe el año estas vacunas puedan obtener el Registro Sanitario”, afirmó. (Con información de la prensa cubana)
















